2020年記事一覧
役員辞任に関するお知らせ
ツーセルでは2つの開発コンセプトを基に、
再生医療等製品の開発に取り組んでいます。
他家間葉系幹細胞(MSC)の利用
患者さん以外のドナーからいただいた(他家)細胞を加工して移植することで、
- 事前に品質のチェックを行えるようになるので、自家移植時に生じ得る「個人差による製品の品質不良」が起こりません。
- ストックすることで、治療が必要になったタイミングで即座に製品を使用することができるようになります。また、自家移植時(患者さんご自身の細胞を用いる治療方法)に必要になる「患者さんご自身からの組織採取手術」が不要です。
- 複数人分の製造を一度で済ませられるため、大量生産・大量供給を通じて製品のコストを下げやすくなります。
MSC用無血清培地STK®シリーズを
使用した細胞培養
ツーセルが目指すのは、再生医療の普及によって
患者さんが
新たな治療法を選択できるようになること
事業
当社の経営理念実現のため再生医療の普及を掲げて、事業に取り組んでいます。現在、再生医療等製品や
再生医療関連製品の研究開発・製造・販売に関する事業を展開しています。
研究開発
当社では、独自の“無血清培地”を使った培養技術を応用して高品質なMSC製品を研究開発しています。
代表例として、パイプラインとその一つであるgMSC®1について下記のページにてご紹介します。
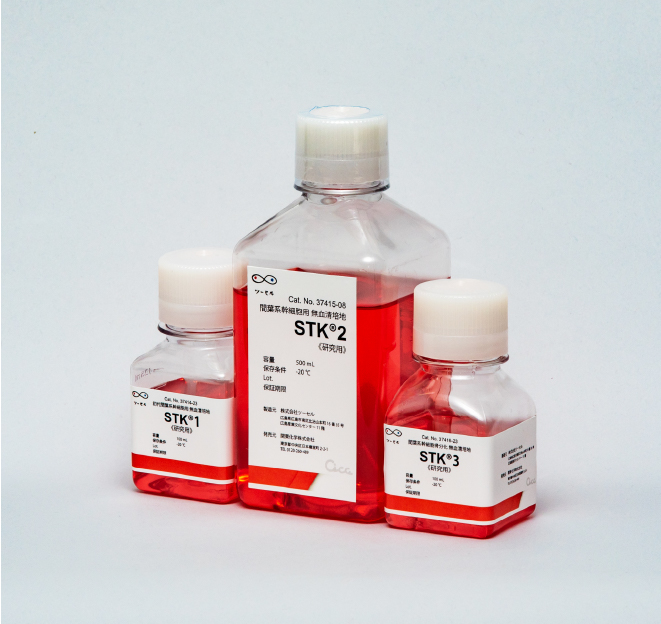
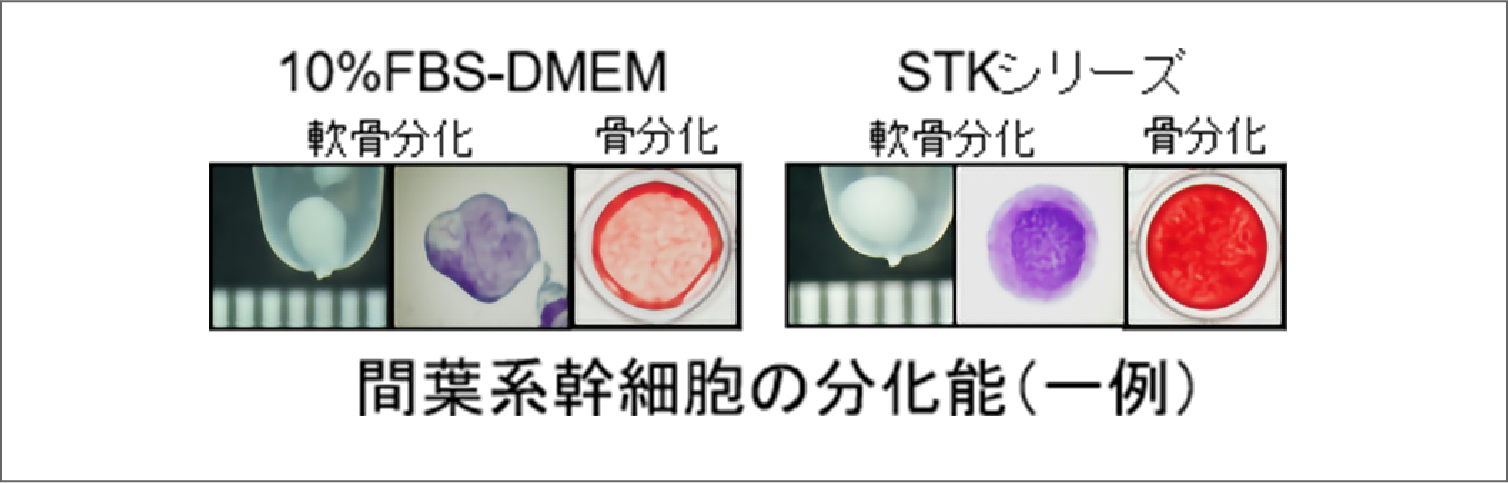
再生医療に使われる細胞は、一般的に自家ヒト血清(患者さん自身の血清)またはウシ胎児血清(以下、FBS)を用いて培養します。しかし、血清成分は多種多様で個人差があり、増殖能力などの品質に大きく影響を与えます。また、FBSの場合個体差だけでなく、動物由来タンパク質へのアレルギーやウイルスの混入などのリスクが発生します。これらのリスクを排除するためには細胞培養を無血清で行うのが理想的と考え、MSC用無血清培地STK®シリーズを開発しました。
STK®シリーズは、血清を用いることなく間葉系幹細胞(以下、MSC)の培養が可能であり、一つ一つの含有成分が特定できているため、安定的に高品質なMSCを作製することが可能です。
- STK®1:初代間葉系幹細胞用 無血清培地
- 骨髄・脂肪・滑膜などの組織から間葉系幹細胞を初代培養するための無血清培地
- STK®2:間葉系幹細胞用 無血清培地
- 間葉系幹細胞の増殖培養用無血清培地
- STK®3:間葉系幹細胞用骨分化用 無血清培地
- 骨分化誘導の効率が高く、最短1週間で骨分化が可能
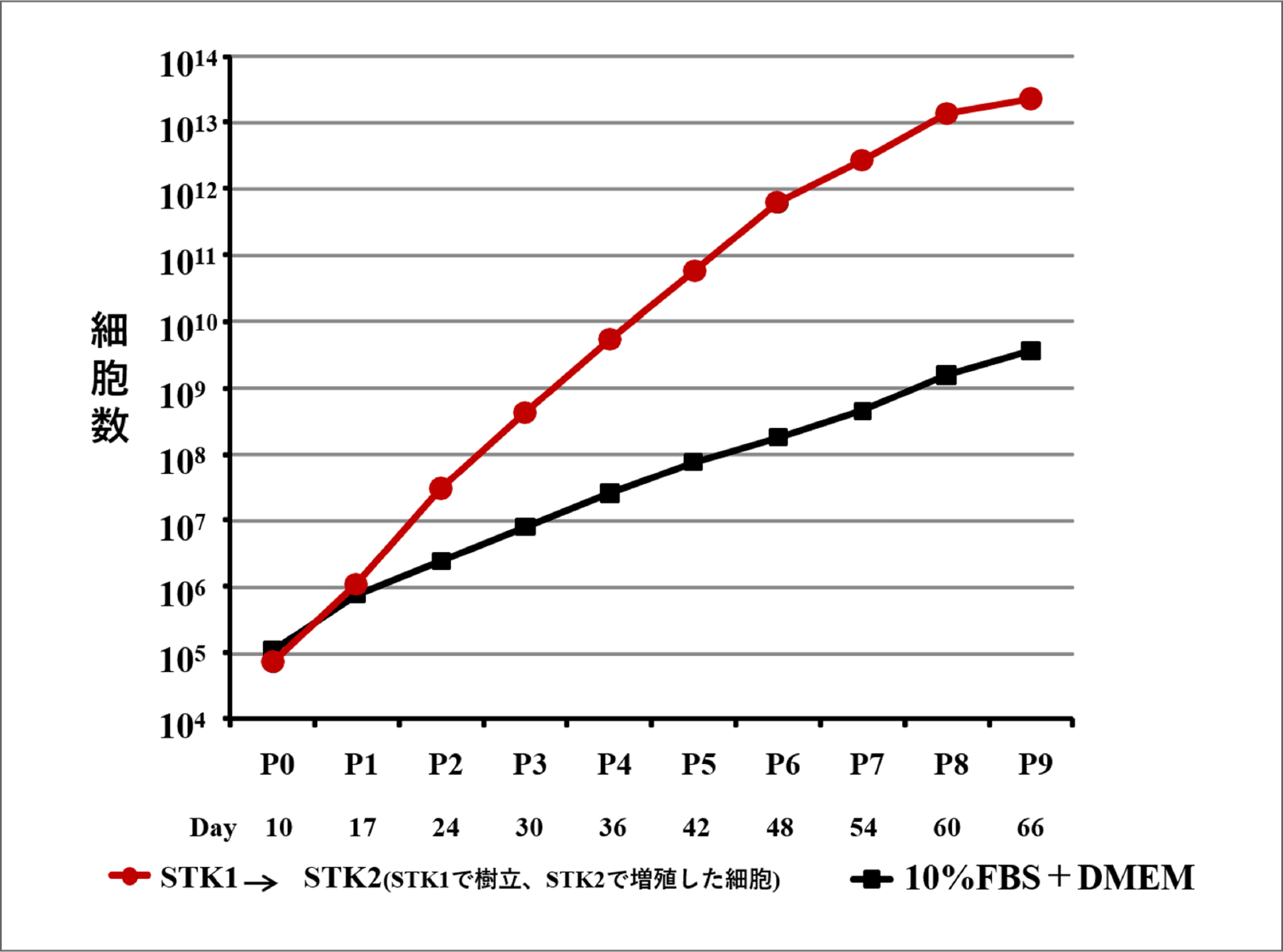
従来の血清添加培地と比べ1,000倍以上の増殖率を達成しました。
臨床研究法
臨床研究法に基づく情報の公開について
臨床研究法に基づく大学等研究機関、病院への資金提供の状況に関する情報開示については、次のとおりです。
gMSC®1は現在開発中の他家由来MSCを
用いた膝軟骨再生細胞治療製品です。
gMSC®1のイメージ
移植細胞用の人工の足場材料(スキャフォールド)を用いる必要がないため安全性が高いこと、豊富な粘着性と柔軟性をもつことから移植部の凹凸にあわせて形状を変えて密着させられることが特徴です。
TECをブタ関節軟骨部欠損モデルに移植したところ、図1のようにTECは移植部に定着し、良好な軟骨再生が観察されており、有害事象も見られませんでした。また、TECは大阪大学での臨床研究によって、その有効性・安全性が確かめられています⁽¹TECを膝軟骨の損傷が認められる被験者に移植したところ、図2のように移植から48週間後には損傷していた膝軟骨部分が軟骨のような組織で覆われていることが観察されています。
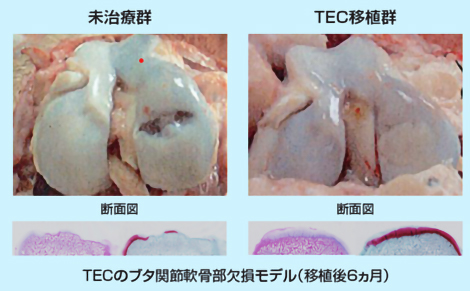 図1
図1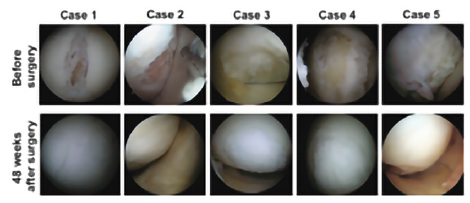 図2
図2データ提供:大阪保健医療大学、大阪大学国際医療情報センター 中村 憲正 先生
gMSC®1ではこのTEC作製技術を応用し、他家滑膜由来MSCを無血清で培養して移植体を作製していることが大きな違いです。
(1:Kazunori S., Norimasa N. et.al., The American Journal of Sports Medicine, 2018 Aug;46(10):2384-2393.
当社独自の無血清培養技術で他家MSCを培養することにより、安定して高品質な製品の大量生産が可能になり、
有効性が証明できれば多くの人の治療が可能になります。
これらの研究開発の結果、中外製薬株式会社と当該領域についてライセンス契約を締結し、2017年より臨床試験を開始しました。
また、gMSC®1の開発においては、製品を冷凍保存する技術を応用することで製造、流通及び医療現場における取り扱いの
簡便性向上を図ることとしています。
細胞を特定の場所で集中生産することで安定した品質の製品を供給し、どの医療機関でも安定で、高品質な再生医療を患者さんに届けることができます。
ツーセルではこのような再生医療の提供方法をセントラル型再生医療事業と名付け、
より多くの患者さんに再生医療を届けようと考えています。
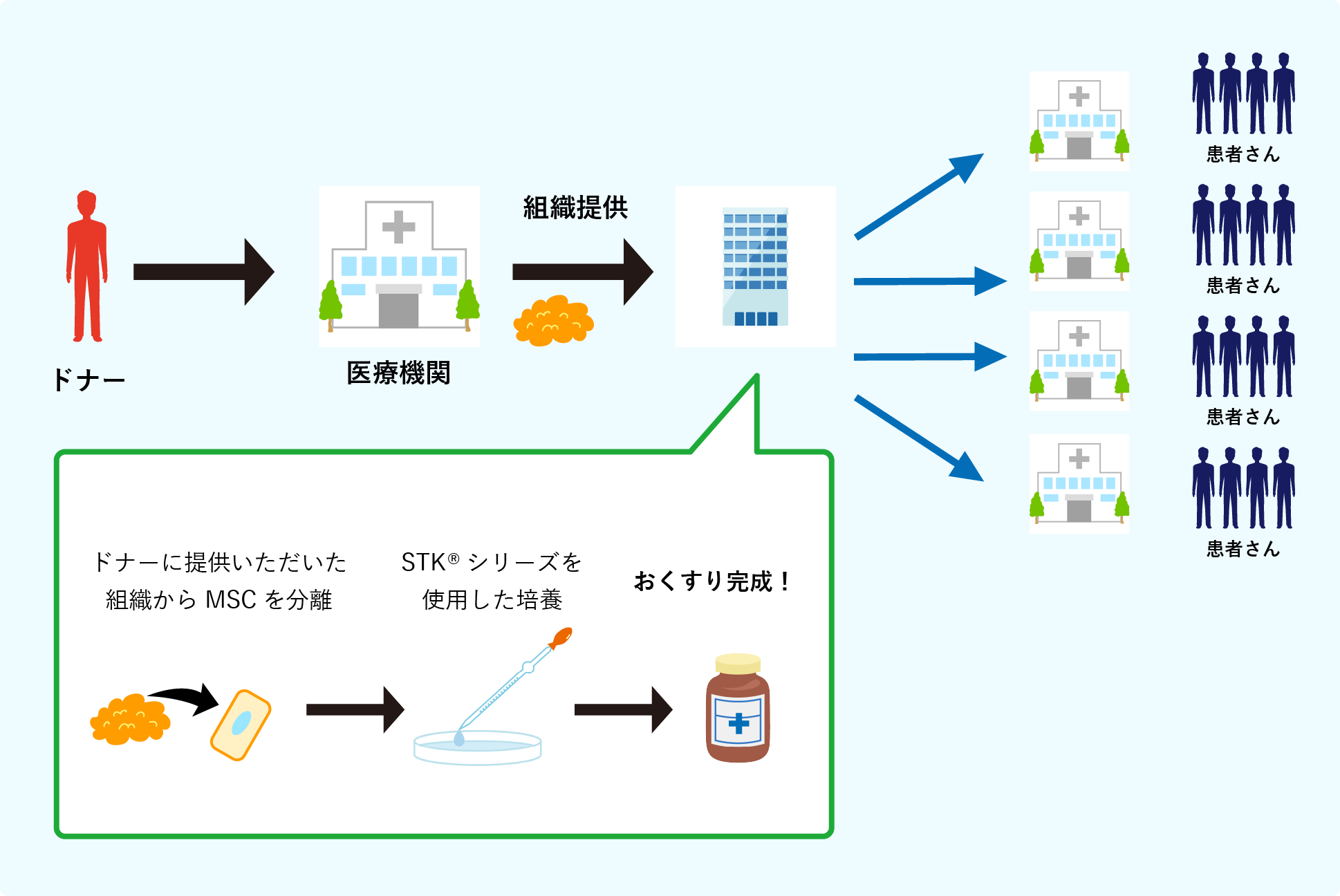

このセントラル型再生医療事業では再生医療で用いられる移植方法である自家移植・他家移植のうち、
他家移植での実施が適しているといわれています。セントラル型再生医療事業の実現に向けた現在開発中の
パイプラインについてはこちらでご紹介しています。
再生医療について
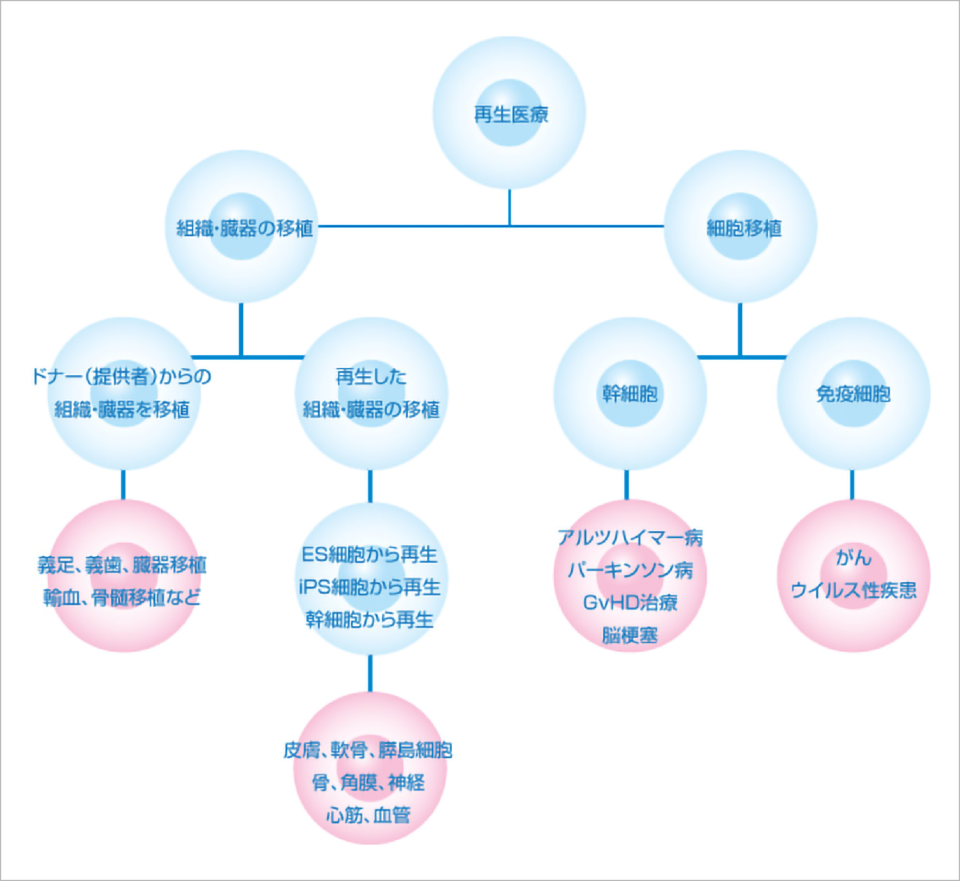
再生医療とは「自然には再生できない組織や臓器を再生させ、
機能を回復させることを目指す医療」です。
人間には元来再生する能力が備わっています。
皮膚は2か月~3か月で新しい細胞に入れ代わり、古くなった皮膚は垢となって脱落します。
同じように胃腸や肺、血管なども数か月をかけて古い細胞が脱落し、
減った分だけ細胞が再生し回復しています。同様に切り傷や骨折も新しい細胞により回復します。
しかし、失っていく細胞の量が再生する細胞の量を超えた時、もとに戻れなくなります。失ったものを自力で補うことができなくなった時、他の力を借りて補う、
という医療が「再生医療」です。義足・義歯、臓器移植、輸血や白血病治療における骨髄移植もそのひとつですし、細胞を血液中に投与したり、細胞により組織を修復したり再生したりする治療もそのひとつです。
これらすべてが再生医療と言われています。
現在、さまざまな細胞を用いた再生医療が研究されています。当社ではそのひとつである「間葉系幹細胞(以下、MSC)を用いた再生医療」に取り組んでいます。MSCを取り出し、体の外で数を増やし、患者さんの体に移植するという治療法です。